Tissue Cytometry技术赋能 Aβ 病理量化 解码 AD 脑内微胶质细胞调控网络
近三十年来,β淀粉样蛋白(Aβ)沉积作为阿尔茨海默病(AD)核心病理特征,始终是疾病干预的关键靶点,基于 Aβ 免疫的治疗策略(含主动免疫与被动免疫)在多项临床试验中展现出降低脑内 Aβ 负荷、延缓认知功能衰退的潜力。利用β淀粉样蛋白(Aβ)免疫的阿尔茨海默病(AD)疗法在临床试验中已显示出潜力。然而,免疫后AD大脑中驱动Aβ清除的机制仍不明确。这些问题严重制约了免疫疗法的优化与疗效提升。

2025年3月,美国西北大学范伯格医学神经基因组学研究中心David Gate教授团队在nature medicine发表题为“Microglial mechanisms drive amyloid-β clearance in immunized patients with Alzheimer’s disease”文章。本研究发现了可增强Aβ靶向免疫疗法的潜在分子靶点,为开发更有效的AD治疗策略开辟了新方向。
本研究采用空间转录组学技术,探究主动和被动Aβ免疫对AD大脑的影响。作者将主动免疫的AD患者与未免疫的AD患者及神经功能健康对照者进行对比,鉴定出与Aβ清除相关的小胶质细胞状态。结合高分辨率空间转录组学与单细胞RNA测序技术,我们深入剖析了仑卡奈单抗(lecanemab)治疗后参与Aβ清除的转录通路,发现小胶质细胞的应答具有空间特异性,且因脑区而异。分析结果显示,两种免疫方式均会导致小胶质细胞中髓系细胞触发受体2(TREM2)和载脂蛋白E(APOE)表达上调,且这两种基因的表达与抗体应答及Aβ清除效率呈正相关。此外,我们证实大脑髓系细胞中的补体信号通路有助于免疫后的Aβ清除。这些发现为阐明调控Aβ清除的转录机制提供了新见解,并揭示了小胶质细胞在免疫介导的Aβ清除中的作用。
实验部分:
Tissue Cytometry技术在该研究中核心作用是为β淀粉样蛋白(Aβ)相关病理分析提供*成像支持,是连接组织形态学与分子机制研究的关键技术:
1. 核心应用场景:Aβ沉积的*成像与量化
研究通过TissueFAXS 系统对经H-DAB染色的脑组织切片进行成像,重点捕获pan-Aβ(全Aβ)染色信号,为后续Aβ沉积分析提供高分辨率原始图像。
成像对象覆盖主动免疫(AN1792疫苗)组、被动免疫(lecanemab抗体)组、未免疫AD组(nAD)及非神经系统疾病对照组(NND)的大脑额叶皮质(FCX)、颞叶皮质(TCX)、顶叶皮质(PCX)和海马体(HIPP)等关键脑区,确保多组学、多区域对比分析的可行性。
2. 关键技术价值:支撑病理量化与分子机制关联
Aβ沉积的*量化:通过去卷积、手动阈值设定、小颗粒干扰去除等步骤,将Aβ染色信号转化,进而计算灰质区域Aβ覆盖率、不同脑区Aβ密度等量化指标,为区分“有限Aβ清除(iAD-lim)”和“广泛Aβ清除(iAD-ext)”表型提供核心依据。
排除干扰因素:通过成像识别血管性Aβ(与脑淀粉样血管病相关)及组织褶皱、孔洞等技术异常区域,在后续分析中排除对应空间转录组斑点(ST spots),确保研究数据的可靠性。
3. 与其他技术的协同:推动多维度机制解析
与空间转录组(ST)、单细胞RNA测序(scRNA-seq)协同:成像获得的Aβ量化数据与ST的基因表达数据叠加,可直接关联Aβ清除程度与microglia(小胶质细胞)等细胞的转录组变化。
与免疫荧光验证互补:成像结果为后续免疫荧光染色(如IBA1+小胶质细胞与Aβ共定位、CD68+溶酶体结构检测)提供靶点区域参考,进一步验证microglia在Aβ清除中的功能作用。
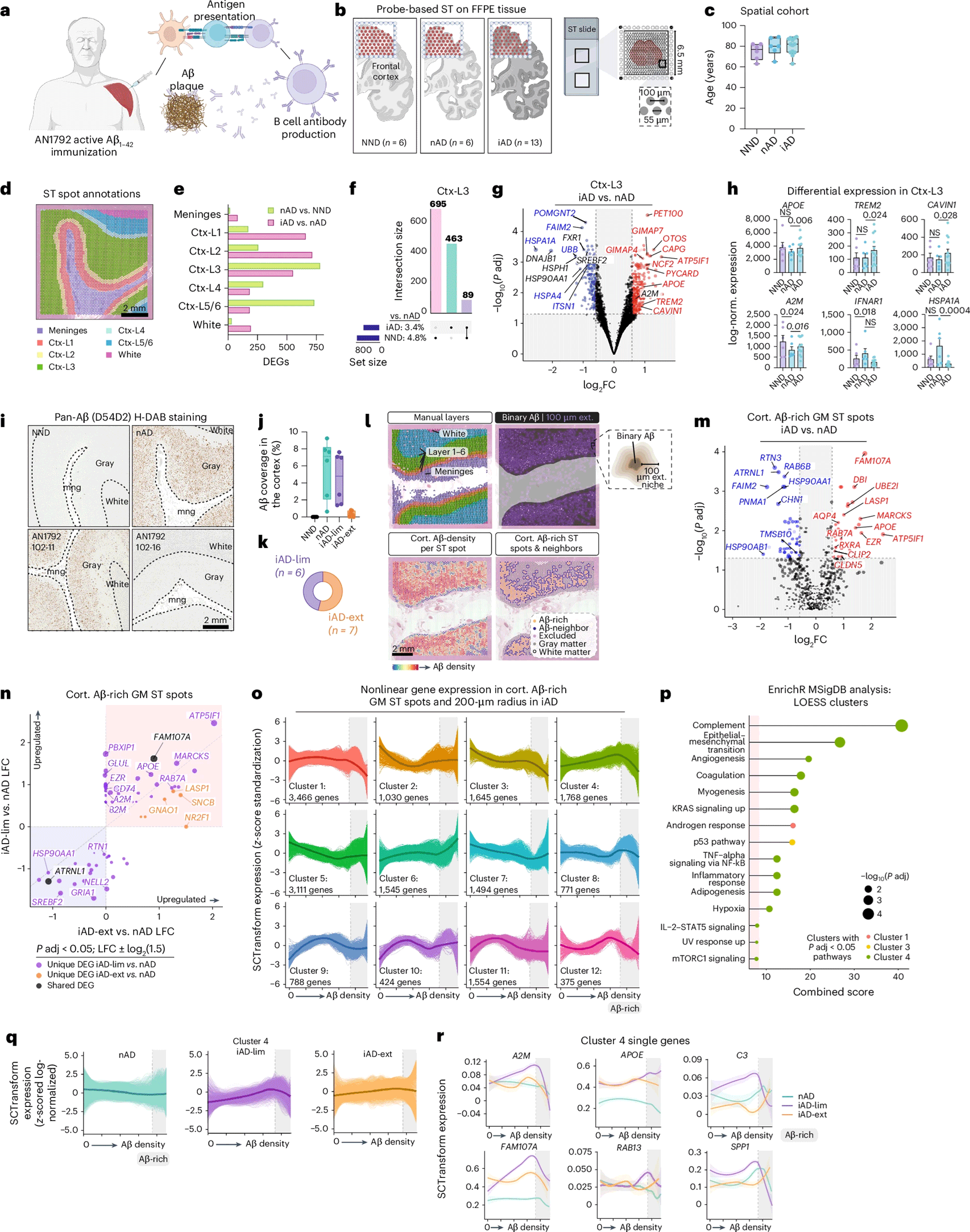
Figure 1 主动 Aβ 免疫可在 Aβ 生态位持续引发炎症。
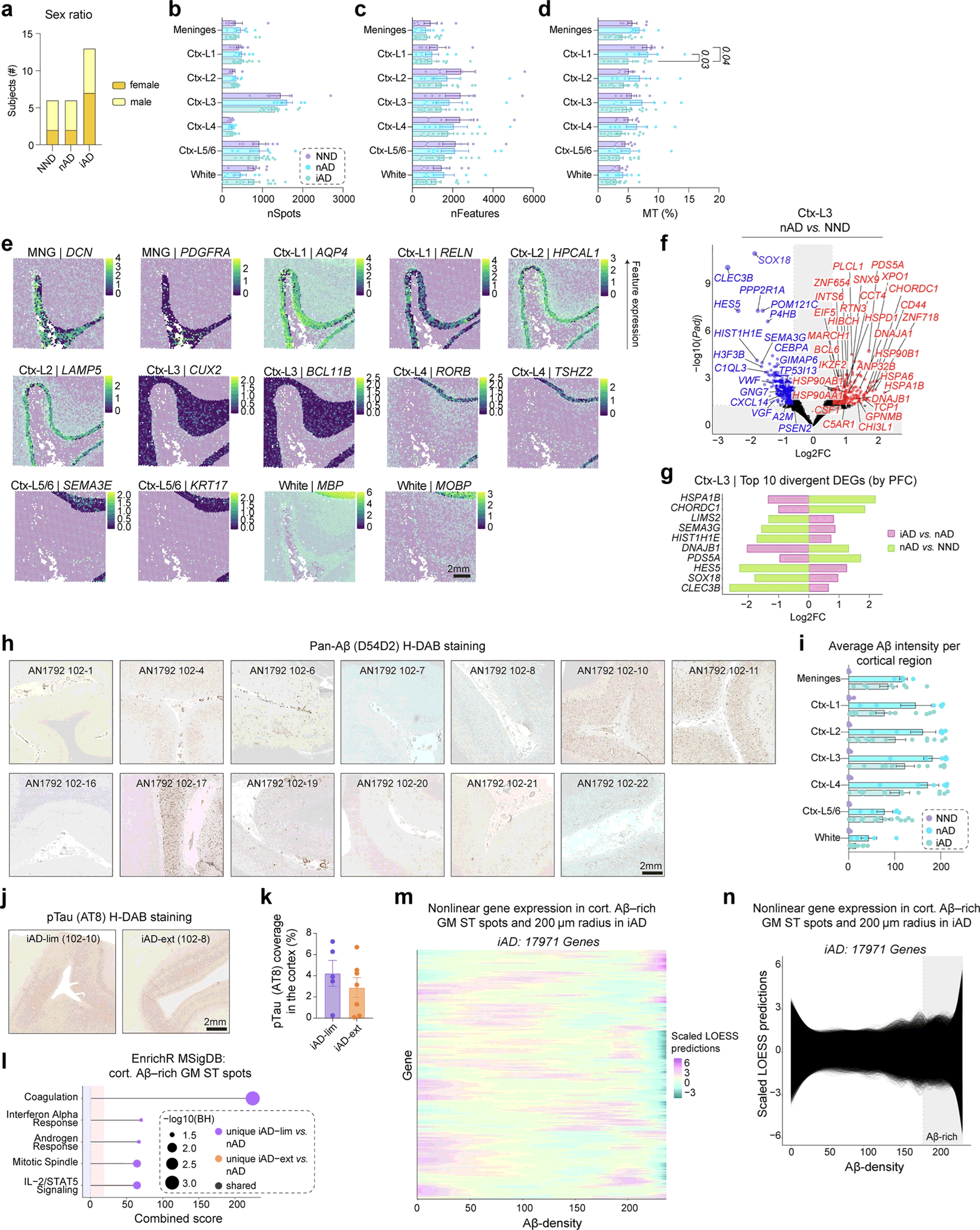
Extend Figure 1 主动 Aβ 免疫可在 Aβ 生态位持续引发炎症。a各组性别分布。

